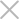国家药监局发布国家医疗器械监督结果 有12批(台)产品不合规定
4月20日,国家药监局关于发布国家医疗器械监督抽检结果的通告,其中德州金约应医疗器械有限公司生产的椎间融合器2批次,表面粗糙度不符合标准规定;半导体激光治疗机1台:CAO Group,Inc. 西尔欧集团生产的半导体激光治疗机标记不符合标准规定;武汉金莱特光电子有限公司生产二氧化碳激光治疗机1台外部标记、控制器件和仪表的准确性、标记不符合标准规定;威海威高医疗影像科技有限公司生产的手持式超声诊断设备外部标记不符合标准规定。
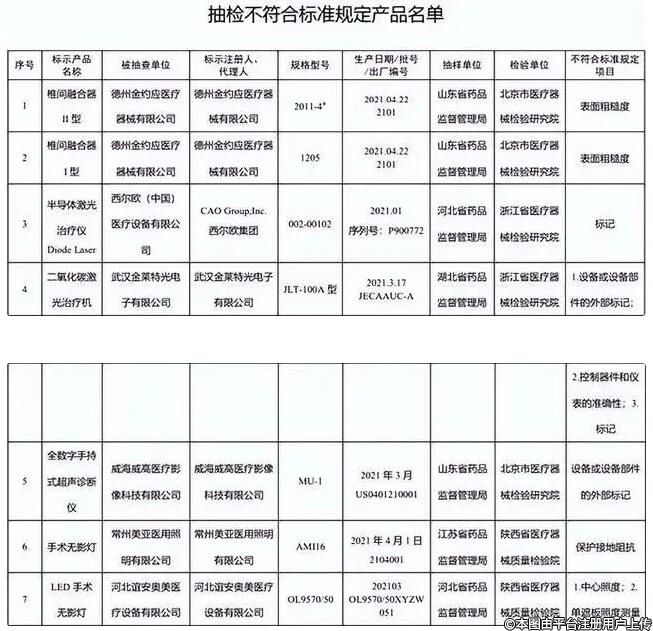
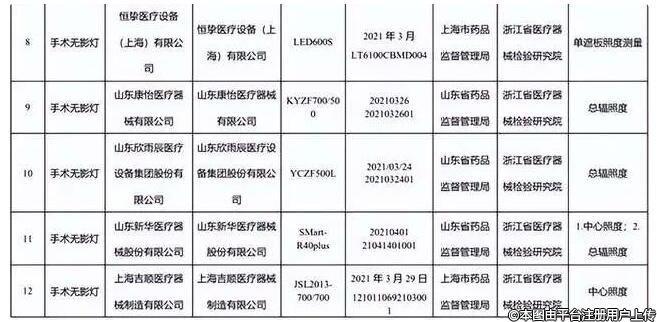
7台手术无影灯分别为山东新华医疗器械股份有限公司、河北谊安奥美医疗设备有限公司、上海吉顺医疗器械制造有限公司等7家企业生产,涉及保护接地阻抗、中心照度、单遮板照度测量、总辐照度等不符合标准规定。
对抽检中发现的不符合标准规定产品,国家药品监督管理局已要求企业所在地省级药品监督管理部门,按照《医疗器械监督管理条例》《医疗器械生产监督管理办法》和《医疗器械召回管理办法》等要求,及时作出行政处理决定并向社会公布。《通告》强调,省级药品监管部门要督促企业对抽检不符合标准规定的产品进行风险评估,根据医疗器械缺陷的严重程度确定召回级别,主动召回产品并公开召回信息;督促企业尽快查明产品不合格原因,制定整改措施并按期整改到位。
文章内容来源:金台资讯
免责说明:本文由网友自由发布,如有侵权,请联系本网站进行删除